胰腺腫瘤位于纖維化組織的緻密層後(hòu)面(miàn),頑固地抵抗治療性分子的遞送。然而,這(zhè)種(zhǒng)屏障,這(zhè)種(zhǒng)增生性腫瘤組織,可以被九個氨基酸的環狀肽iRGD穿透。在胰腺癌模型的實驗中,特别是在小鼠模型和類器官的實驗中,發(fā)現iRGD通過(guò)β5整合素介導的分子途徑穿透腫瘤,β5整合素是一種(zhǒng)由癌相關的成(chéng)纖維細胞(CAF)産生的蛋白質。這(zhè)一新發(fā)現的β5整合素的作用表明,該蛋白可以作爲一種(zhǒng)有用的生物标志物,可以表明哪些患者對(duì)iRGD和化療藥物聯合治療産生最佳反應。
這(zhè)項新發(fā)現來自加州大學(xué)聖地亞哥分校(UCSD)醫學(xué)院和Moores癌症中心的研究人員與Sanford Burnham Prebys醫學(xué)發(fā)現研究所和哥倫比亞大學(xué)的研究人員合作進(jìn)行的一項研究。Moores癌症中心腫瘤外科主任AndrewLowy醫學(xué)博士說(shuō):“從我們的研究中獲得的知識有可能(néng)直接應用于病人護理。我們還(hái)認爲胰腺癌中β5整合素的水平可以告訴我們哪些患者從iRGD聯合治療中受益最大。”
他們發(fā)表于《Nature Communications》上的論文“Tumor-penetrating therapy for β5 integrin-rich pancreas cancer”報道(dào)了CAFs以TGF-β依賴的方式誘導腫瘤細胞中β5整合素的表達,使其成(chéng)爲腫瘤穿透肽iRGD的有效藥物遞送靶點。

文章作者寫道(dào):“當腫瘤細胞中β5整合素被敲除時(shí),iRGD傳遞結合和共注入有效載荷的能(néng)力被顯著抑制。值得注意的是,腫瘤細胞中β5整合素的敲除可減少疾病負擔,延長(cháng)小鼠的生存期,證明其對(duì)PDAC進(jìn)展的貢獻。”
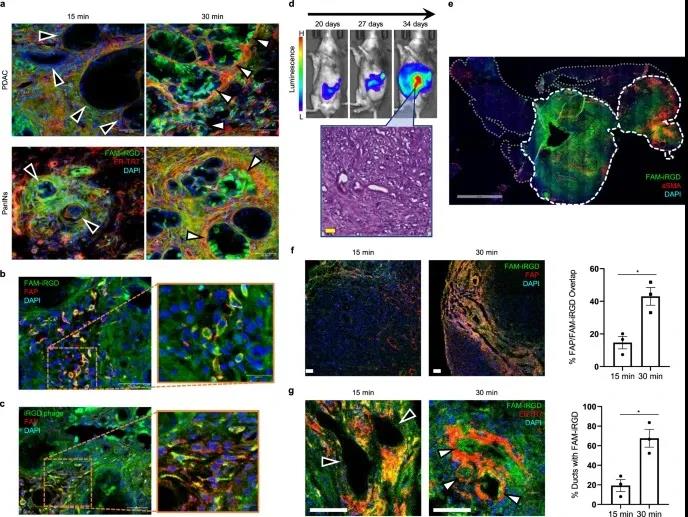
PCAD,或稱胰腺導管腺癌,是胰腺癌的一種(zhǒng)亞型,其高度耐藥性部分歸因于腫瘤周圍的硬殼狀外層。在美國(guó),每12分鍾就(jiù)有一個人死于胰腺癌,而胰腺癌被确診時(shí)通常已是晚期。它傳播迅速,五年生存率約爲10%。治療方法可能(néng)包括放療、手術和化療,盡管癌症通常會(huì)對(duì)藥物産生耐藥性。
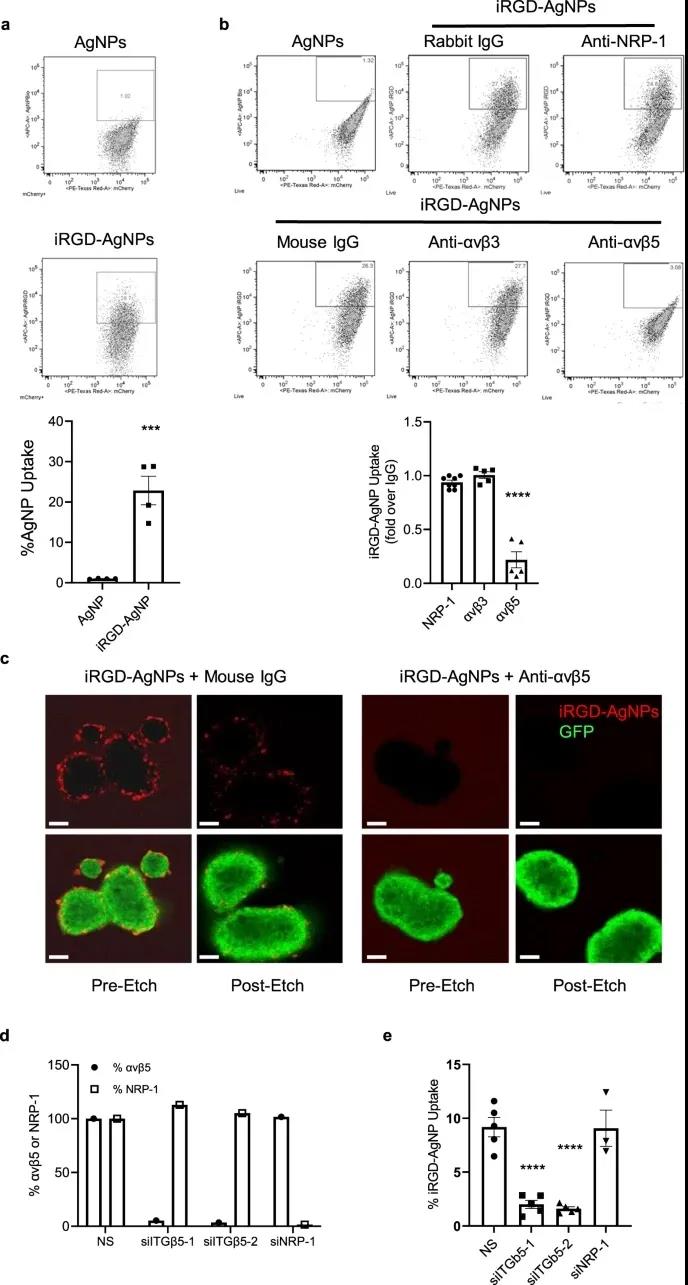
根據這(zhè)項新的研究,被稱爲iRGD的腫瘤穿透肽似乎能(néng)增強化療的效果,減少轉移,提高生存率,其程度取決于β5整合素的水平。從本質上講,β5整合素爲化療藥物提供了從内部破壞腫瘤的機會(huì)。
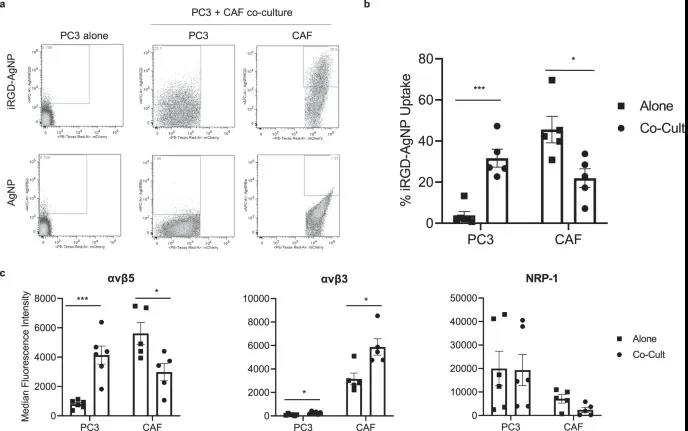
“這(zhè)種(zhǒng)腫瘤是由密集的纖維組織組成(chéng)的,它是藥物試圖通過(guò)的屏障。”研究人員解釋說(shuō),“很多藥物都(dōu)能(néng)到達腫瘤血管,但無法深入組織,使治療效果降低,這(zhè)也是爲什麼(me)這(zhè)種(zhǒng)癌症治療如此具有挑戰性的原因之一。”
“我們的研究發(fā)現,腫瘤穿透肽iRGD能(néng)夠利用這(zhè)種(zhǒng)纖維網絡將(jiāng)化療藥物輸送到腫瘤的深處,而且更有效。”
研究小組在小鼠模型中檢測了PDAC腫瘤的微環境。他們發(fā)現在靶向(xiàng)腫瘤血管後(hòu),iRGD與高水平的β5整合素結合,β5整合素是由CAFs産生的一種(zhǒng)蛋白質,CAFs是産生腫瘤大部分保護性纖維覆蓋層的細胞。
研究人員說(shuō):“我們能(néng)夠在我們的小鼠模型中緊密複制人類疾病,并發(fā)現當給β5整合素水平高的小鼠注射iRGD進(jìn)行化療時(shí),與單純化療相比,存活率顯著提高,癌細胞擴散到體内其它器官的幾率也顯著降低。這(zhè)可能(néng)是一種(zhǒng)針對(duì)侵襲性胰腺癌的有效治療策略。”
“這(zhè)個發(fā)現同樣令人興奮的是iRGD療法沒(méi)有産生任何其它的副作用。在考慮對(duì)患者進(jìn)行治療時(shí),這(zhè)一點至關重要。”
研究人員說(shuō),下一步將(jiāng)包括一項全國(guó)性的人體臨床試驗。他們估計試驗可能(néng)在一年内開(kāi)始。“随著(zhe)iRGD的臨床研究進(jìn)入下一階段,”文章作者總結道(dào),“基于iRGD結合蛋白(尤其是β5整合素)作爲假定生物标志物的表達譜的患者分層將(jiāng)是非常有趣和重要的。”
----------THE END----------
免責聲明:本文系轉載分享,文章觀點、内容、圖片及版權歸原作者所有,如涉及侵權請聯系删除!